Un nemico subdolo: la corrosione in barca
Tra le tante insidie a bordo, la corrosione è forse la più subdola: pericolosa e invisibile, rappresenta una vera minaccia per ogni imbarcazione. Per evitarla, è quindi bene conoscerla e riconoscerla.
Con questo approfondimento, il nostro proposito è quello di fornire una panoramica sulle varie tipologie di corrosione e sulle relative cause, insieme a qualche utile suggerimento per combatterla.
La corrosione a bordo può essere di diversi tipi: semplice, galvanica (la più diffusa) o elettrolitica (la più aggressiva). Ci sono anche altri tipi di corrosione, che citiamo per completezza, ma che non esamineremo, poiché è molto raro che si verifichino sulle imbarcazioni da diporto: corrosione per cavitazione — che riguarda le eliche in moto veloce — per sfregamento meccanico e per attacco chimico.
Tra tutti i fenomeni che un armatore deve tenere sotto controllo a bordo della propria barca, la corrosione è la più insidiosa: attacca silenziosamente e in maniera graduale. Soprattutto, non risparmia alcuna parte dell’imbarcazione: dallo scafo al fuoribordo, tutto è in pericolo.
CORROSIONE SEMPLICE: COS’È E COME RISOLVERLA
Questo tipo di corrosione inizia quando il metallo comincia ad arrugginire una volta tirato fuori dall’acqua. Vi suona familiare? È proprio ciò che spesso accade ai motori fuoribordo. In questo caso, è possibile combattere la corrosione avendo molta cura del proprio motore e mantenendolo pulito: basta lavarlo con un detergente apposito e poi proteggerlo con prodotti specifici per motori marini.
CORROSIONE GALVANICA
Per quanto riguarda la corrosione galvanica, la questione è un po’ più complessa, ma in generale avviene quando due elementi metallici, in contatto elettrico tra loro, si arrugginiscono o corrodono.
Questa corrosione dipende da un fenomeno del tutto naturale, che Alessandro Volta concretizzò con la creazione dell’omonima pila. In parole povere, come funziona una pila di Volta? Il suo principio si basa sul fatto che ogni metallo possiede un proprio potenziale elettrico, che varia da un metallo all’altro; senza addentrarci troppo nelle leggi della fisica, basta sapere che da una differenza di potenziale elettrico (o tensione) nasce una corrente elettrica. Dunque, se colleghiamo due metalli con potenziali elettrici differenti, si genera una differenza di potenziale e, di conseguenza, una corrente elettrica che scorrerà dal metallo con potenziale maggiore al metallo con potenziale minore. Perché ci interessa tutto ciò? Perché una pila di Volta costituita da soli due elementi metallici è, in effetti, una cella galvanica.
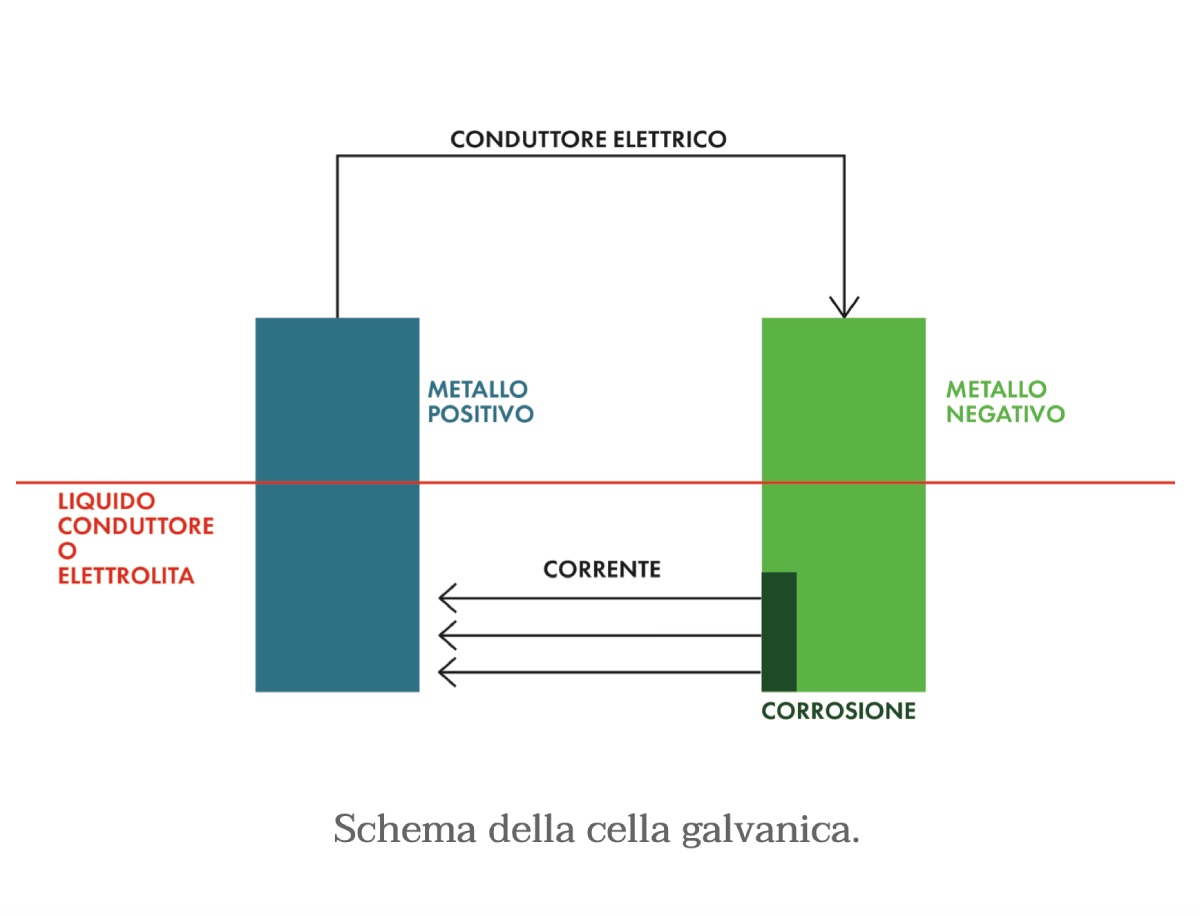
È importante capire cosa serve affinché si realizzi una cella galvanica, perché conoscere la sua composizione ci aiuterà nella nostra crociata contro la corrosione galvanica. La cella galvanica si realizza se – e solo se – sono presenti tutti e tre i seguenti elementi:
– Due metalli differenti;
– Un liquido conduttore (elettrolita) a contatto con entrambi i metalli. Non è necessario che i due metalli siano entrambi immersi nell’elettrolita, ma dovranno essere a contatto con lo stesso liquido conduttore, anche in quantità minima;
– Un collegamento elettrico tra i due metalli.
Da questa prima infarinatura, possiamo già trarre alcune conclusioni. Innanzitutto, le barche nei laghi si corrodono meno perché l’acqua dolce è un elettrolita meno efficiente rispetto all’acqua di mare. In secondo luogo, occorre ricordare di evitare l’uso di ottone comune a contatto con l’acqua salata. Perché? L’ottone è una lega composta principalmente da rame e zinco. Lo zinco ha un potenziale elettrochimico più basso nella scala galvanica; di conseguenza, se un pezzo di ottone viene immerso in acqua di mare — che funge da elettrolita — si innesca un processo di dezincificazione che porta, nel tempo, alla formazione di una struttura porosa di rame, con la perdita dello zinco e il conseguente deterioramento dell’ottone.
Inoltre, occorre tenere presente che l’intensità della corrente galvanica è direttamente proporzionale alla differenza di potenziale tra i metalli coinvolti: maggiore è tale differenza, maggiore sarà la corrente elettrica e, di conseguenza, più rapida e intensa sarà la corrosione.
Un altro elemento da considerare è il rapporto tra le superfici dei due elementi metallici. Facciamo un esempio prendendo un rivetto e una lastra: il rivetto ha ovviamente una superficie molto minore rispetto alla lastra. Supponiamo ora che il rivetto sia in alluminio (metallo meno nobile, anodo) e la lastra in acciaio (metallo più nobile, catodo): il rivetto si corroderà visibilmente e in tempi molto brevi. Al contrario, se il rivetto fosse in acciaio e la lastra in alluminio, la corrosione risulterebbe molto meno significativa in rapporto alla superficie.
Per questo motivo, è sempre preferibile utilizzare rivetti o viti realizzati in metalli più nobili rispetto al materiale in cui vengono inseriti.

COME AFFRONTARE LA CORROSIONE GALVANICA
Alla luce di quanto appena descritto, sembrerebbe che la soluzione più semplice per evitare la corrosione galvanica sia impedire la formazione di una cella galvanica: poiché sono necessari tre elementi affinché essa si realizzi, è sufficiente che ne manchi uno. Tuttavia, non è possibile evitare del tutto che questo fenomeno avvenga; pensiamo, ad esempio, all’elettrolita: basterebbe l’assenza del liquido conduttore affinché la cella non si formi, quindi la soluzione ideale sarebbe mantenere tutto asciutto.
Mantenere tutto asciutto a bordo di una barca che naviga in acque salate, però, non è un compito semplice. Tuttavia, è possibile adottare alcuni accorgimenti:
– Non utilizzare metalli molto distanti nella serie galvanica in sentina e sotto la linea di galleggiamento;
– Scegliere viti e bulloni realizzati in metalli più nobili rispetto ai materiali che vanno a fissare;
– Non impiegare lubrificanti contenenti grafite, poiché essa è nobile rispetto alla maggior parte dei metalli;
– In presenza di un collegamento elettrico in banchina, avvalersi sempre di un isolatore galvanico;
– Tenere isolati tra loro metalli diversi;
– Utilizzare un ritorno della corrente elettricamente isolato.
GLI ANODI SACRIFICALI
Non abbiamo ancora parlato dei nostri migliori alleati in questa battaglia: gli anodi sacrificali. Il nome parla da sé: sono elementi realizzati in materiale poco nobile (solitamente zinco) che vengono accoppiati ad altri materiali in modo da sacrificarsi e corrodersi al posto dell’elemento metallico da proteggere. Possono essere posizionati in varie zone dell’imbarcazione, dallo scafo al motore.
Grazie a un controllo regolare degli anodi, è possibile assicurarsi che questi stiano svolgendo correttamente il loro compito, sostituendoli quando il loro peso si è ridotto di circa il 50%. Occorre tuttavia prestare attenzione: se gli anodi si corrodono troppo rapidamente, è necessario individuarne la causa; se invece non si corrodono affatto, ciò non è un buon segno e potrebbe indicare che non stanno svolgendo correttamente la loro funzione, ad esempio perché non sono posizionati in modo adeguato.
Come accennato, solitamente gli anodi sacrificali sono realizzati in zinco, tanto che talvolta vengono chiamati “zinchi sacrificali”. Tuttavia, possono essere anche in magnesio o in alluminio, a seconda delle condizioni di utilizzo: in acqua dolce si impiegano anodi in magnesio; gli anodi in alluminio possono essere utilizzati su imbarcazioni anche metalliche, purché non realizzate in alluminio. Se sono presenti strutture in alluminio, non si devono utilizzare anodi sacrificali in magnesio, poiché si può causare una sovraprotezione che porta alla corrosione dell’alluminio.
CORROSIONE ELETTROLITICA: LA PIÙ TEMIBILE
La corrosione elettrolitica è detta anche corrosione da correnti vaganti. Osservando lo schema utilizzato in precedenza per rappresentare la cella galvanica, si noterà che il metallo che subisce la corrosione è quello da cui esce la corrente convenzionale. Tuttavia, un metallo può corrodersi anche senza far parte di una cella galvanica tradizionale. Com’è possibile? È sufficiente che la differenza di potenziale tra due metalli sia generata da una forza elettromotrice esterna.
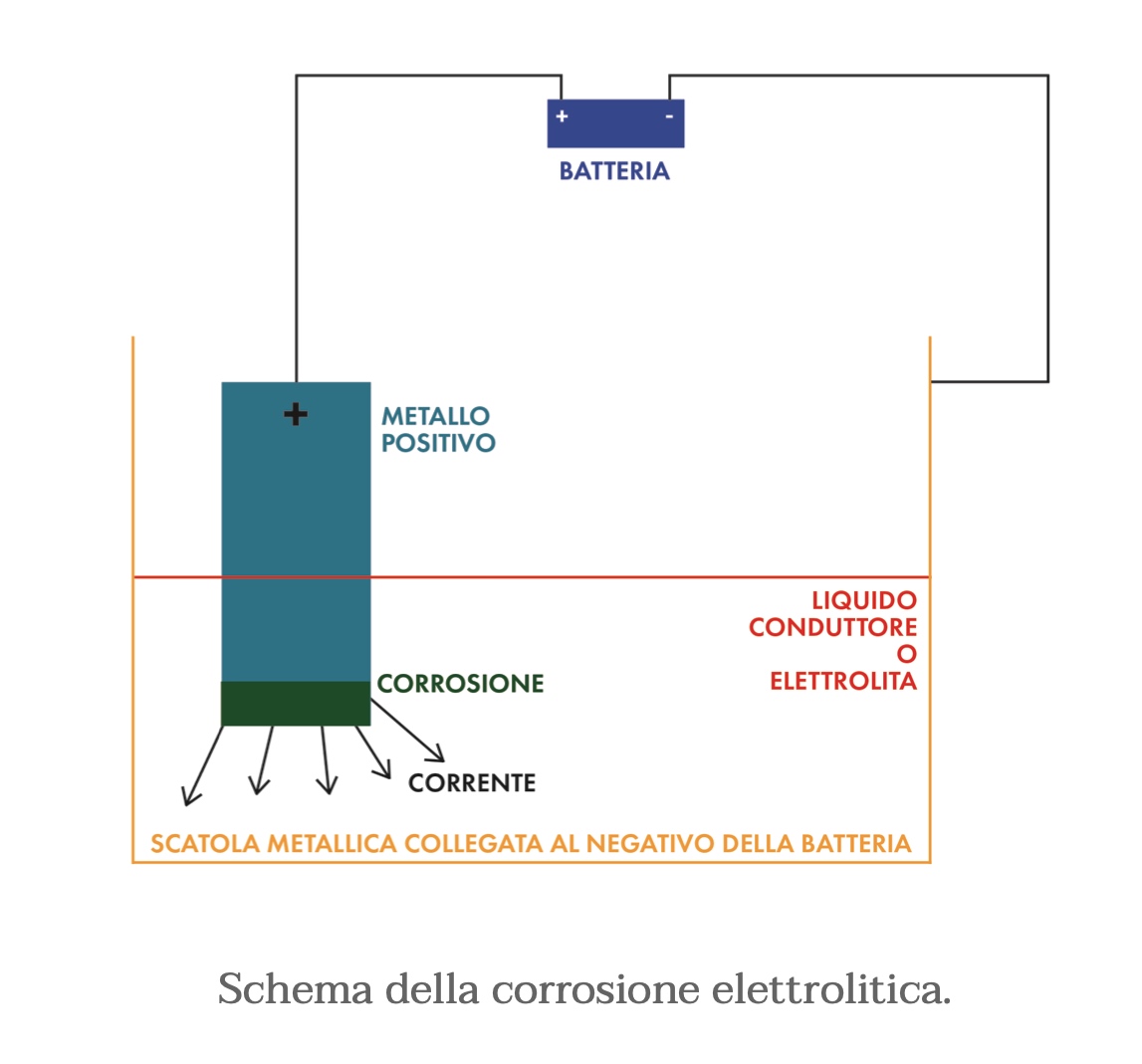
Consideriamo una scatola metallica riempita con un elettrolita e una barra di un altro metallo immersa nel liquido. Applicando una differenza di potenziale mediante una sorgente esterna, ad esempio una batteria, il metallo immerso viene portato a potenziale positivo e si genera una corrente che, grazie all’elettrolita, fluisce verso la scatola metallica e ritorna al polo negativo. In questo modo, come già visto, sarà la barra immersa a corrodersi, poiché è il corpo dal quale la corrente esce.
La corrosione da correnti vaganti è particolarmente pericolosa, se possibile più della corrosione galvanica: è infatti più rapida e più devastante, poiché le differenze di potenziale in gioco sono generalmente molto più elevate. Questo tipo di corrosione è solitamente sintomo di un problema elettrico, sia a bordo dell’imbarcazione sia a livello della banchina, ed è causato da dispersioni di corrente nei cavi che collegano la batteria alle utenze.
Purtroppo, gli anodi sacrificali non sono efficaci contro questo tipo di corrosione. L’unico modo per prevenirla è disporre di un impianto elettrico di bordo correttamente progettato, ben cablato e privo di difetti o falsi contatti.






